摘要:目的 促進委托生產(chǎn)的藥品上市許可持有人(MAH)持續(xù)改進和提升質(zhì)量管理體系�����,確保能生產(chǎn)出符合注冊要求的藥品�����。方法對安徽省2021 年至2025 年委托生產(chǎn)的MAH 申請《藥品生產(chǎn)質(zhì)量管理規(guī)范》(GMP)符合性檢查情況進行匯總與分析�����,總結(jié)存在的問題�����,并提出有針對性的建議�����。結(jié)果共受理并檢查89 家次委托生產(chǎn)的MAH 申請的上市前GMP 符合性檢查�����,有6 家次(6.74%)的檢查結(jié)論為不符合要求?����,F(xiàn)場檢查共發(fā)現(xiàn)缺陷831 項�����,平均每家次9. 34 項�����,其中嚴(yán)重缺陷6 項(0.72%)�����,主要缺陷74 項(8.90%)�����,一般缺陷751 項(90.37%)�����;檢查缺陷項目主要集中在質(zhì)量控制與質(zhì)量保證(23.59%)、文件管理(19.13%)�����、委托生產(chǎn)與委托檢驗(12.27%)�����、機構(gòu)與人員(9.87%)等方面�����。缺陷存在的原因主要有質(zhì)量管理人員履職能力不足�����,質(zhì)量管理體系不完善�����,質(zhì)量監(jiān)督力度較弱�����,委托方與受托方質(zhì)量管理體系銜接不暢�����。結(jié)論委托生產(chǎn)的MAH 在開展委托生產(chǎn)時應(yīng)合理選擇受托生產(chǎn)企業(yè)�����,建立有效的溝通機制�����,采取有效措施改進質(zhì)量管理體系�����,強化生產(chǎn)全過程的監(jiān)督�����,增強風(fēng)險防控意識�����,確保所生產(chǎn)的藥品安全�����、有效。
藥品上市許可持有人(MAH)是指取得藥品注冊證書的企業(yè)或藥品研制機構(gòu)等可自行生產(chǎn)藥品�����,也可委托具備條件的藥品生產(chǎn)企業(yè)生產(chǎn)�����。MAH獲得藥品上市許可后通過《藥品生產(chǎn)質(zhì)量管理規(guī)范》(GMP)符合性檢查后方可上市銷售�����。GMP符合性檢查是指藥品監(jiān)督管理部門依據(jù)法律法規(guī)對MAH�����、藥品生產(chǎn)企業(yè)的生產(chǎn)和質(zhì)量管理活動開展的檢查活動�����。委托生產(chǎn)的MAH 的GMP符合性檢查是指MAH獲得委托生產(chǎn)品種上市許可后需進行的上市前GMP符合性檢查�����。本研究中總結(jié)了安徽省委托生產(chǎn)的MAH在接受GMP符合性檢查過程中存在的問題�����,并提出有針對性的改進建議�����,為委托生產(chǎn)的MAH有效提升質(zhì)量管理水平提供參考?����,F(xiàn)報道如下�����。
1 申請情況
1. 1 檢查依據(jù)
《藥品注冊管理辦法》[1]第四十七條規(guī)定�����,對于創(chuàng)新藥�����、改良型新藥�����、生物制品等,應(yīng)進行上市前GMP檢查�����;第四十七條規(guī)定�����,對于仿制藥等�����,根據(jù)是否已獲得相應(yīng)生產(chǎn)范圍的藥品生產(chǎn)許可證且已有同劑型品種上市等情況�����,基于風(fēng)險進行上市前GMP 檢查�����;第四十八條規(guī)定�����,上市前GMP檢查的管理要求�����,按《藥品生產(chǎn)監(jiān)督管理辦法》的有關(guān)規(guī)定執(zhí)行�����?����!端幤飞a(chǎn)監(jiān)督管理辦法》[2]第十六條規(guī)定�����,原址或異地新建�����、改建�����、擴建車間或生產(chǎn)線的應(yīng)進行GMP符合性檢查�����;第五十二條規(guī)定,未通過與生產(chǎn)該藥品的生產(chǎn)條件相適應(yīng)的GMP符合性檢查的品種�����,應(yīng)進行上市前的GMP 符合性檢查�����;第五十三條�����、第五十五條對生產(chǎn)監(jiān)督檢查的主要內(nèi)容及相關(guān)檢查的頻次進行了規(guī)定�����?����!端幤飞鲜泻笞兏芾磙k法(試行)》[3]第八條規(guī)定�����,轉(zhuǎn)讓的藥品在通過GMP符合性檢查后�����,符合產(chǎn)品放行要求的,可上市銷售�����;第十四條對MAH藥品生產(chǎn)場地變更進行了規(guī)定�����?����!端幤窓z查管理辦法(試行)》[4]第三十五條規(guī)定�����,申請藥品上市的�����,按《藥品生產(chǎn)監(jiān)督管理辦法》第五十二條的規(guī)定�����,根據(jù)需要開展上市前的GMP符合性檢查�����。藥品批準(zhǔn)證明文件載明“藥品生產(chǎn)企業(yè)應(yīng)當(dāng)符合《藥品生產(chǎn)質(zhì)量管理規(guī)范》要求方可生產(chǎn)銷售”的�����,MAH也應(yīng)提交上市前GMP符合性檢查申請�����。
1. 2 申請情況
截至2025年9月1日�����,安徽省持有B類藥品生產(chǎn)許可證(委托生產(chǎn))的MAH共93家�����,申請GMP符合性檢查的有34 家(36. 56%)�����;34 家申請GMP 符合性檢查的MAH中,僅有B類生產(chǎn)許可范圍的有24家(70. 59%)�����;34 家MAH 共涉及89 家次上市前GMP 符合性檢查申請�����。本研究中主要分析委托生產(chǎn)的MAH 申請上市前GMP符合性檢查事項發(fā)現(xiàn)的缺陷�����,不包含中藥飲片�����、原料藥及按GMP 符合性檢查開展的藥品生產(chǎn)許可事項等�����。經(jīng)統(tǒng)計�����,委托生產(chǎn)的MAH申請開展上市前GMP符合性檢查類型見表1�����。
2 檢查情況
2. 1 總體情況
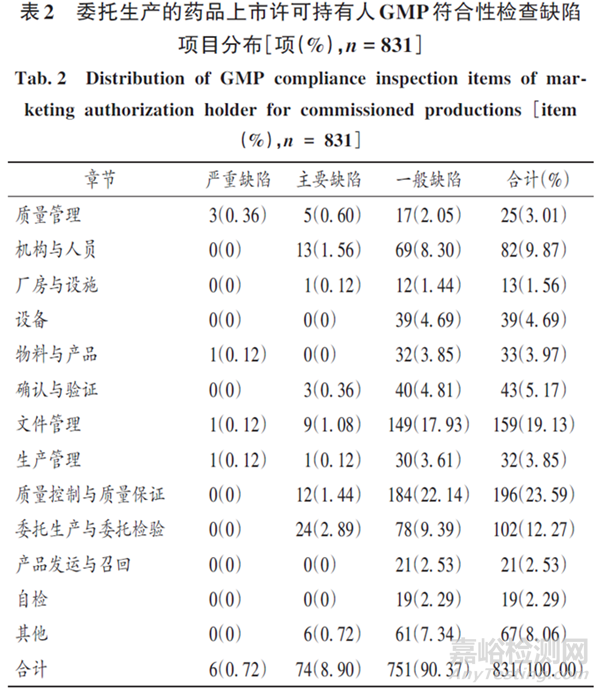
2021年1月至2025年8月�����,安徽省共受理并檢查了89家次委托生產(chǎn)的MAH申請的上市前GMP符合性檢查�����。89家次GMP符合性檢查涉及54家受托生產(chǎn)企業(yè)�����,其中22 家(40.74%)為本省內(nèi)的藥品生產(chǎn)企業(yè)�����;涉及150個委托生產(chǎn)品種�����,其中高風(fēng)險委托生產(chǎn)品種40個(26.67%)�����;赴省內(nèi)受托生產(chǎn)企業(yè)同步開展GMP符合性檢查的有42家次(47.19%)。通過對現(xiàn)場檢查報告進行審核�����、研判�����,有6家次(6.74%)GMP符合性檢查的結(jié)論不符合要求�����,其中4家次MAH僅有B類藥品生產(chǎn)許可證?����,F(xiàn)場檢查共發(fā)現(xiàn)缺陷831項�����,平均每家次9.34項�����,其中嚴(yán)重缺陷6項(0.72%)�����,主要缺陷74項(8.90%)�����,一般缺陷751項(90.37%)�����;赴省內(nèi)受托生產(chǎn)企業(yè)開展的檢查共發(fā)現(xiàn)缺陷425項�����,平均每家次10.12項�����,其中嚴(yán)重缺陷2項(4.70%)�����,主要缺陷58項(13.65%)�����,一般缺陷365項(85.88%)。根據(jù)GMP及其附錄章節(jié)進行劃分�����,檢查缺陷主要集中在質(zhì)量控制與質(zhì)量保證(23.59%)�����、文件管理(19.13%)�����、委托生產(chǎn)與委托檢驗(12.27%)�����、機構(gòu)與人員(9.87%)�����。詳見表2�����。
2. 2 缺陷情況
2. 2. 1 嚴(yán)重缺陷情況
嚴(yán)重缺陷是指與GMP要求有嚴(yán)重偏離�����,產(chǎn)品可能對使用者造成危害的缺陷[5]�����。GMP符合性檢查現(xiàn)場檢查時發(fā)現(xiàn)的嚴(yán)重缺陷主要體現(xiàn)在質(zhì)量保證方面與GMP要求有較大偏離�����,導(dǎo)致質(zhì)量保證體系不能有效運行�����。如MAH未對駐廠人員資質(zhì)進行審核確認(rèn)�����,駐廠人員不能有效履職�����;受托方審計報告內(nèi)容簡單�����,缺少質(zhì)量控制實驗室、生產(chǎn)設(shè)施設(shè)備�����、檢驗設(shè)施設(shè)備的審計內(nèi)容�����;未對原料供應(yīng)商進行審計�����;雙方成品質(zhì)量標(biāo)準(zhǔn)限度規(guī)定不一致�����;關(guān)鍵崗位人員職責(zé)未按《藥品上市許可持有人落實藥品質(zhì)量安全主體責(zé)任監(jiān)督管理規(guī)定》及時修訂�����;未按要求制訂藥物警戒體系主文件�����;受托方制訂的產(chǎn)品工藝規(guī)程有誤�����,實際生產(chǎn)工藝與再注冊工藝不一致�����;雙方不能及時�����、有效地識別重大變更�����、中等變更等�����。GMP符合性檢查綜合審評時發(fā)現(xiàn)的嚴(yán)重缺陷主要為駐廠質(zhì)量保證(QA)人員已離職并入職其他企業(yè)�����,MAH未如實相告�����,并讓離職人員在現(xiàn)場迎檢。
2. 2. 2 主要缺陷情況
主要缺陷是指與GMP要求有較大偏離的缺陷[5]�����。從檢查缺陷分布情況看�����,主要缺陷體現(xiàn)在質(zhì)量控制與質(zhì)量保證�����、文件管理�����、機構(gòu)與人員�����、委托生產(chǎn)與委托檢驗�����,具體缺陷如下。
質(zhì)量控制與質(zhì)量保證方面:1)變更管理典型缺陷�����。物料供應(yīng)商變更后�����,物料的出廠質(zhì)量標(biāo)準(zhǔn)與受托方的內(nèi)控質(zhì)量標(biāo)準(zhǔn)存在差異未識別�����;藥品生產(chǎn)場地變更前后�����,產(chǎn)品的投料量�����、折算方式�����、關(guān)鍵生產(chǎn)設(shè)備發(fā)生變更�����,MAH未能識別�����。2)供應(yīng)商管理典型缺陷�����。供應(yīng)商檔案不全�����,未按要求對原輔料供應(yīng)商進行審計�����。3)質(zhì)量控制典型缺陷�����。原始檢驗記錄所附薄層色譜圖上的取樣點位置標(biāo)注不清晰�����,薄層色譜展開斑點模糊,高效液相色譜圖有明顯肩峰等�����。
文件管理方面:委托雙方的文件未按藥品委托生產(chǎn)質(zhì)量協(xié)議約定內(nèi)容進行修訂�����,如偏差處理�����、變更控制�����、糾正與預(yù)防措施�����、回收�����、返工�����、重新加工等�����;受托方制訂的委托產(chǎn)品工藝規(guī)程�����、批生產(chǎn)記錄內(nèi)容不詳細(xì)�����;受托方制訂的產(chǎn)品質(zhì)量標(biāo)準(zhǔn)�����、檢驗操作規(guī)程與注冊資料不一致等�����。
機構(gòu)與人員方面:1)人員履職典型缺陷�����。未發(fā)現(xiàn)產(chǎn)品工藝驗證方案中確認(rèn)范圍和報告數(shù)據(jù)的合理性不足;未發(fā)現(xiàn)清潔驗證方案中缺少必要的生產(chǎn)設(shè)備�����,清潔驗證指標(biāo)不準(zhǔn)確�����,清潔驗證方法中取樣�����、檢驗方法與已驗證的方法不一致�����;生產(chǎn)負(fù)責(zé)人未參與產(chǎn)品生產(chǎn)工藝規(guī)程的審核或批準(zhǔn)等�����;未對受托方成品微生物限度檢驗方法的驗證方案及報告進行審核等�����。2)人員配備典型缺陷�����。未配備質(zhì)量控制(QC)人員�����;藥物警戒負(fù)責(zé)人資質(zhì)不符合要求�����;委托產(chǎn)品是無菌藥品�����,質(zhì)量受權(quán)人無無菌藥品生產(chǎn)和質(zhì)量管理實踐經(jīng)驗等�����。
委托生產(chǎn)與委托檢驗方面:質(zhì)量協(xié)議前后內(nèi)容不一致�����,照搬照抄模板內(nèi)容與實際情況不相符�����,未明確物料放行的責(zé)任方,批號的制訂與實際制訂不一致�����,物料實際采購方與協(xié)議約定不一致�����,全權(quán)由受托方確定委托檢驗機構(gòu)�����,并簽訂委托檢驗協(xié)議等�����。
3 缺陷存在原因分析
3. 1 質(zhì)量管理人員履職能力不足
本研究中分析的34家委托生產(chǎn)的MAH中�����,有24家(70.59%)為藥品研發(fā)類機構(gòu)或藥品經(jīng)營類機構(gòu)的MAH�����,高層管理人員更關(guān)注產(chǎn)品能否盡快上市銷售�����、集中帶量采購能否中標(biāo)入選等生存指標(biāo)[6-7]�����,若質(zhì)量管理部門在組織機構(gòu)中層級偏低�����、無話語權(quán)�����,則更難推進質(zhì)量管理向好發(fā)展�����。部分法定代表人為控制成本�����,限定在職人員數(shù)量�����,返聘離崗多年的退休人員擔(dān)任質(zhì)量受權(quán)人、質(zhì)量負(fù)責(zé)人�����、生產(chǎn)負(fù)責(zé)人等關(guān)鍵崗位�����,人員匹配不足�����,關(guān)鍵崗位人員知識更新不足�����,不能順應(yīng)藥品生產(chǎn)質(zhì)量管理的需求�����,變更�����、偏差�����、藥物警戒等質(zhì)量管理概念不強�����,不能有效辨識質(zhì)量風(fēng)險�����,更有甚者不能有效保證工作的順利開展�����。
3. 2 質(zhì)量管理體系不完善
由表2可見�����,“質(zhì)量管理”的嚴(yán)重缺陷最多�����,“質(zhì)量控制與質(zhì)量保證”的缺陷總數(shù)最多�����。據(jù)檢查員反饋,不知如何搭建委托生產(chǎn)質(zhì)量管理體系是企業(yè)反映最多的問題�����。實際上�����,自我國從法律層面上確定MAH制度以來�����,有關(guān)部門相繼發(fā)布了《藥品上市許可持有人檢查要點(征求意見稿)》[8]�����、《藥品委托生產(chǎn)質(zhì)量協(xié)議指南(2020年版)》[9]�����、《藥品上市許可持有人落實藥品質(zhì)量安全主體責(zé)任監(jiān)督管理規(guī)定》[10]�����、《關(guān)于加強藥品上市許可持有人委托生產(chǎn)監(jiān)督管理工作的公告》[11]�����、《藥品上市許可持有人委托生產(chǎn)現(xiàn)場檢查指南》[12]�����、《藥品共線生產(chǎn)質(zhì)量風(fēng)險管理指南》[13]�����、《北京市藥品上市許可持有人委托生產(chǎn)藥品生產(chǎn)質(zhì)量管理規(guī)范符合性檢查要點(試行)(征求意見稿)》[14]�����,雖然以上公告�����、指南�����、征求意見稿不具有強制性�����,但細(xì)化的要求對于MAH如何搭建委托生產(chǎn)質(zhì)量管理體系具有較高的指導(dǎo)意義。關(guān)鍵崗位人員不關(guān)注MAH制度的最新動態(tài)�����,不研讀相關(guān)的公告�����、指南�����,不愿去主動完善質(zhì)量管理體系�����;另外�����,變更控制�����、偏差管理、自檢�����、外審等流于形式�����,得過且過�����,導(dǎo)致委托生產(chǎn)質(zhì)量體系不健全或與實際情況不相符�����,不能有效控制產(chǎn)品質(zhì)量的風(fēng)險�����。
3. 3 質(zhì)量監(jiān)督力度較弱
委托生產(chǎn)的MAH應(yīng)對藥品委托生產(chǎn)全過程進行指導(dǎo)和監(jiān)督�����。大多數(shù)MAH希望通過派駐人員或單純記錄審核來實現(xiàn)對委托產(chǎn)品的質(zhì)量監(jiān)督�����,實際能否達(dá)到預(yù)期結(jié)果�����,值得質(zhì)疑�����。檢查中發(fā)現(xiàn)�����,駐廠人員的監(jiān)督記錄不全面�����,不能實現(xiàn)對全過程的監(jiān)督�����;監(jiān)督記錄不詳細(xì)�����,不能體現(xiàn)對關(guān)鍵工藝參數(shù)的確認(rèn);監(jiān)督記錄流于形式�����,用“是”與“否”進行確認(rèn)�����,不能達(dá)到監(jiān)督的效果�����。
3. 4 委托方與受托方質(zhì)量管理體系銜接不暢
委托生產(chǎn)的MAH 和受托生產(chǎn)企業(yè)是2 家不同企業(yè)�����,會存在企業(yè)文化�����、質(zhì)量管理風(fēng)格�����、對同樣異常情況的認(rèn)識與處置等不同情況�����。委托與受托雙方的質(zhì)量管理體系銜接不暢�����,各自為政�����,較為普遍�����。如某一受托生產(chǎn)企業(yè)發(fā)現(xiàn)受托產(chǎn)品某一工序的注冊工藝與自持相似品種的某一工序處理方式不一致�����,未向MAH匯報�����,擅自按自持相似品種處理方式進行生產(chǎn)�����,進而導(dǎo)致委托生產(chǎn)產(chǎn)品的實際生產(chǎn)工藝與注冊工藝不一致。
缺乏必要的質(zhì)量信息溝通也是雙方質(zhì)量管理體系銜接不暢的表現(xiàn)�����。委托雙方在實際委托生產(chǎn)過程中僅圍繞委托產(chǎn)品的質(zhì)量管理風(fēng)險進行溝通�����,受托方不會主動匯報由企業(yè)生產(chǎn)的其他品種暴露出的質(zhì)量共性問題�����,MAH也不會關(guān)注�����,那么委托生產(chǎn)的品種可能就會存在質(zhì)量風(fēng)險隱患�����。
4 建議
4. 1 重視質(zhì)量管理
建議委托生產(chǎn)的MAH重視質(zhì)量管理[15]�����,在組織機構(gòu)上提高質(zhì)量管理部門的地位�����,提供充實的人力資源�����,定期聽取質(zhì)量管理工作匯報�����,并提出意見�����,推進相關(guān)問題的解決�����,以確保質(zhì)量管理工作的開展�����。加大人員培訓(xùn)力度�����,并考核培訓(xùn)效果,考核結(jié)果與績效�����、職稱晉升掛鉤�����。制訂具體的考評細(xì)則�����,多次考核不過關(guān)的堅決不用�����,尤其是關(guān)鍵崗位人員�����。全員應(yīng)重視自檢�����、外審�����、管理評審等質(zhì)量保證手段�����,盡可能地找出產(chǎn)品存在的風(fēng)險�����,不能走過場�����。全員提高產(chǎn)品生產(chǎn)質(zhì)量持續(xù)合規(guī)的敏銳性�����,不能無視產(chǎn)生的變更�����,亦不可刻意降低變更等級�����,建議MAH持續(xù)學(xué)習(xí),并關(guān)注國家藥品監(jiān)督管理局出臺的法規(guī)�����、指導(dǎo)原則�����、指南等�����。
4. 2 強化生產(chǎn)全過程監(jiān)督
委托生產(chǎn)的MAH對委托生產(chǎn)的監(jiān)督應(yīng)在統(tǒng)籌生產(chǎn)全過程的基礎(chǔ)上把握質(zhì)量關(guān)鍵點�����,及時�����、準(zhǔn)確地發(fā)現(xiàn)委托生產(chǎn)過程中出現(xiàn)的異常情況�����。建議制訂合理的監(jiān)督記錄�����,確保實現(xiàn)有效監(jiān)督�����。法規(guī)中要求生物制品�����、中藥注射劑�����、多組分生化藥的委托生產(chǎn)必須派駐人員�����,其他產(chǎn)品的委托生產(chǎn)未作要求�����,建議有條件的MAH委托生產(chǎn)期間安排有生產(chǎn)和質(zhì)量管理經(jīng)驗的人員駐廠�����。集團內(nèi)的委托生產(chǎn),建議MAH要求受托生產(chǎn)企業(yè)賦予一定的信息管理系統(tǒng)權(quán)限�����,便于質(zhì)量監(jiān)督�����。
4. 3 合理選擇受托生產(chǎn)企業(yè)
6家次GMP符合性檢查不通過中有2家次是涉及同一MAH和同一受托生產(chǎn)企業(yè)�����,故合理選擇受托生產(chǎn)企業(yè)是保障委托生產(chǎn)產(chǎn)品質(zhì)量至關(guān)重要的環(huán)節(jié)�����。黃哲等[16]和張冉等[17]構(gòu)建了MAH伙伴選擇模型�����,他們認(rèn)為需從商務(wù)協(xié)同�����、生產(chǎn)質(zhì)量�����、企業(yè)管理�����、財務(wù)狀況�����、交貨保證方面綜合評價受托生產(chǎn)企業(yè)�����。建議委托生產(chǎn)的MAH選擇省內(nèi)委托�����、集團內(nèi)委托�����,質(zhì)優(yōu)的受托生產(chǎn)企業(yè)更能保障委托生產(chǎn)品種的質(zhì)量�����。
4. 4 建立有效溝通機制
建議在藥品委托生產(chǎn)質(zhì)量管理協(xié)議中明確質(zhì)量溝通的方式、頻次�����,結(jié)合各自質(zhì)量管理體系細(xì)化約定內(nèi)容�����,達(dá)成共識的內(nèi)容應(yīng)盡量包含所有質(zhì)量管理活動�����,并明確界定雙方的責(zé)任和義務(wù)�����。建議通過信息化手段進行委托生產(chǎn)過程中質(zhì)量信息的溝通�����,以解決信息傳遞失真�����、溝通不暢等問題。
4. 5 完善GMP 附錄
自GMP的2010年修訂版實施以來�����,我國共頒布了13個附錄�����,分別為無菌藥品附錄�����、原料藥附錄�����、生物制品附錄�����、血液制品附錄�����、中藥制劑附錄�����、放射性藥品附錄�����、中藥飲片附錄�����、醫(yī)用氧附錄�����、取樣附錄�����、計算機化附錄�����、確認(rèn)與驗證附錄�����、生化藥品附錄、臨床試驗用藥品附錄�����。附錄內(nèi)容更具有針對性�����,條款更細(xì)化�����,有利于企業(yè)完善藥品生產(chǎn)質(zhì)量管理體系�����。建議國家藥品監(jiān)督管理局頒布MAH(委托生產(chǎn))附錄�����,便于委托生產(chǎn)的MAH開展GMP符合性檢查工作�����。
5 結(jié)語
上市前的藥品GMP 符合性檢查是委托生產(chǎn)的MAH所持藥品走向公眾的最后一個關(guān)鍵環(huán)節(jié)�����,若生產(chǎn)質(zhì)量管理存在問題�����,可能會導(dǎo)致不合格產(chǎn)品流入市場�����,帶來用藥安全風(fēng)險�����。據(jù)報道�����,某MAH委托生產(chǎn)品種的含量抽檢不合格被北京市市場監(jiān)督管理局責(zé)令停產(chǎn)停業(yè)整頓并罰款[18]�����,這一行政處罰警示我們�����,作為藥品安全第一責(zé)任人的MAH,應(yīng)加強委托生產(chǎn)期間的藥品生產(chǎn)質(zhì)量管理�����,切實保障藥品生命周期全過程的安全性�����、有效性及質(zhì)量可控性�����,確保受托生產(chǎn)企業(yè)能持續(xù)生產(chǎn)出符合注冊要求的產(chǎn)品�����,以保障患者的用藥安全�����。
參考文獻
[1]國家市場監(jiān)督管理總局. 藥品注冊管理辦法[A / OL].(2020 - 01 - 22)[2024 - 09 - 29]. https:// www. samr. gov.cn / zw / zfxxgk / fdzdgknr / fgs / art / 2023 / art_3275cb2a929d4c34ac8c0421b2a9c257. html.
[2]國家市場監(jiān)督管理總局. 藥品生產(chǎn)監(jiān)督管理辦法[A / OL].(2020 - 01 - 22)[2024 - 09 - 29]. https:// www. samr. gov.cn / zw / zfxxgk / fdzdgknr / fgs / art / 2023 / art_65070d0ee03a4109ac831ee7b3cee51c. html.
[3]國家藥品監(jiān)督管理局. 關(guān)于發(fā)布《藥品上市后變更管理辦法(試行)》的公告[A / OL].(2021 - 01 - 13)[2024 - 09 - 29].https:// www. nmpa. gov. cn / xxgk / fgwj / xzhgfxwj / 20210113142301136. html.
[4]國家藥品監(jiān)督管理局. 關(guān)于修訂《藥品檢查管理辦法(試行)》部分條款有關(guān)事宜的通知[A / OL].(2023 - 07 - 21)[2024 - 09 - 29]. https:// www. nmpa. gov. cn / xxgk / fgwj /gzwj / gzwjyp / 20230721091201181. html.
[5]國家食品藥品監(jiān)督管理總局. 關(guān)于印發(fā)藥品生產(chǎn)現(xiàn)場檢查風(fēng)險評定指導(dǎo)原則的通知[A / OL].(2014 - 05 - 13)[2024 -09 - 29]. https:// www. nmpa. gov. cn / xxgk / fgwj / gzwj / gzwjyp/ 20140513120001350. html.
[6]左武劍�����,李新天. 僅委托生產(chǎn)的藥品上市許可持有人質(zhì)量管理的現(xiàn)狀調(diào)研分析[J]. 中國藥事�����,2024�����,38(7):745 - 751.
[7]姚煒凱�����,陳航�����,吳聲楊�����,等. 福建省藥品上市許可持有人委托生產(chǎn)檢查現(xiàn)狀分析[J]. 中國藥業(yè)�����,2024�����,33(2):15 - 18.
[8]國家藥品監(jiān)督管理局綜合司. 公開征求《藥品上市許可持有人檢查工作程序(征求意見稿)》《藥品上市許可持有人檢查要點(征求意見稿)》意見[A / OL].(2020 - 03 - 02)[2024 - 09 - 29]. https:// www. nmpa. gov. cn / xxgk / zhqyj /zhqyjyp / 20200302155401756. html.
[9]國家藥品監(jiān)督管理局. 關(guān)于發(fā)布藥品委托生產(chǎn)質(zhì)量協(xié)議指南(2020年版)的公告[A/OL].(2020-09-27)[2024-09- 29].https:// www. nmpa. gov. cn / xxgk / ggtg / ypggtg / ypqtggtg /20201009174033199. html.
[10]國家藥品監(jiān)督管理局. 關(guān)于發(fā)布《藥品上市許可持有人落實藥品質(zhì)量安全主體責(zé)任監(jiān)督管理規(guī)定》的公告[A / OL].(2022 - 12 - 29)[2024 - 09 - 29]. https:// www. nmpa.gov. cn / xxgk / fgwj / xzhgfxwj / 20221229195805180. html.
[11]國家藥品監(jiān)督管理局. 關(guān)于加強藥品上市許可持有人委托生產(chǎn)監(jiān)督管理工作的公告[A / OL].(2023 - 10 - 23)[2024 - 09 - 29]. https:// www. nmpa. gov. cn / xxgk / fgwj /xzhgfxwj / 20231023160426145. html.
[12]國家藥品監(jiān)督管理局綜合司. 關(guān)于印發(fā)藥品上市許可持有人委托生產(chǎn)現(xiàn)場檢查指南的通知[A / OL].(2023 - 10 - 24)
[2024 - 09 - 29]. https:// www. nmpa. gov. cn / xxgk / fgwj /gzwj / gzwjyp / 20231024161543188. html.
[13]國家藥品監(jiān)督管理局食品藥品審核查驗中心. 關(guān)于發(fā)布《藥品共線生產(chǎn)質(zhì)量風(fēng)險管理指南》的通告[A / OL].(2023 -03 - 06)[2024 - 09 - 29]. https:// www. cfdi. org. cn / resource/ news / 15186. html.
[14]北京市藥品監(jiān)督管理局. 關(guān)于對《北京市藥品上市許可持有人委托生產(chǎn)藥品質(zhì)量管理規(guī)范符合性檢查要點(試行)(征求意見稿)》公開征集意見的公告[A/OL].(2021- 06- 09)[2024 - 09 - 29]. https:// yjj. beijing. gov. cn / yjj / zwhd17 /zjdc38 / 11008090 / index. html.
[15]孫京林,余伯陽. 藥品上市許可持有人制度下的質(zhì)量管理體系[J]. 中國藥學(xué)雜志�����,2020�����,55(23):1919 - 1922.
[16]黃哲�����,陳宇�����,李慧. 藥品上市許可持有人伙伴選擇研究[J]. 哈爾濱商業(yè)大學(xué)學(xué)報(社會科學(xué)版)�����,2018(6):63-71.
[17]張冉�����,宋明月�����,武志昂�����,等. 藥品上市許可持有人委托生產(chǎn)受托方選擇質(zhì)量風(fēng)險管理研究[J]. 中國藥業(yè)�����,2021�����,30(17):1 - 6.
[18]張悅�����,曹學(xué)平. 藥品不合格朗迪制藥被罰1. 3億元[EB/OL].(2023 - 10 - 21)[2024 - 09 - 29]. https:// baijiahao. baidu.com / s�����?id = 1780361112384576895&wfr = spider&for = pc.