嚙齒類動物致癌性研究結果陽性,接下來該怎么辦�����?很多朋友都提出這類疑問����,略作分享����。
一、陽性結果≠終止研發(fā)
一項在FDA數(shù)據(jù)庫中對282種人類藥物(其中229種已上市)的回顧分析發(fā)現(xiàn)�,44.3%的化合物在長期致癌性試驗中呈現(xiàn)陽性結果���。類似地,在德國和荷蘭提交上市申請的藥物中�,近50%曾提交過陽性致癌性研究報告,且通常大鼠比小鼠更敏感����。
這說明,動物致癌性試驗陽性并不等于該藥物對人體具有致癌風險�,也不意味著必須終止開發(fā)。
關鍵在于:判斷這種腫瘤效應是否在人類中具有相關性�����。
大多數(shù)具有遺傳毒性的化合物會在早期研發(fā)階段被篩除���,一般不會進入致癌性試驗。但存在例外情況�����,例如用于治療癌癥或其他危及生命的疾病的藥物,其臨床獲益可能遠大于潛在致癌風險����。
盡管已有學者質疑傳統(tǒng)2年嚙齒類動物致癌性試驗在預測人體風險方面的價值�����,并提出替代策略�,但本文重點不在于討論這些替代方法�,而是聚焦于如何應對非遺傳毒性化合物在致癌性研究中的陽性發(fā)現(xiàn),并科學評估其對人體的潛在風險��。
二、核心應對策略:開展作用機制(MOA)分析
當致癌性研究出現(xiàn)陽性結果時��,首要任務是:闡明腫瘤發(fā)生的生物學機制(Mechanism of Action,MOA)�����,并評估該機制是否適用于人類�����。
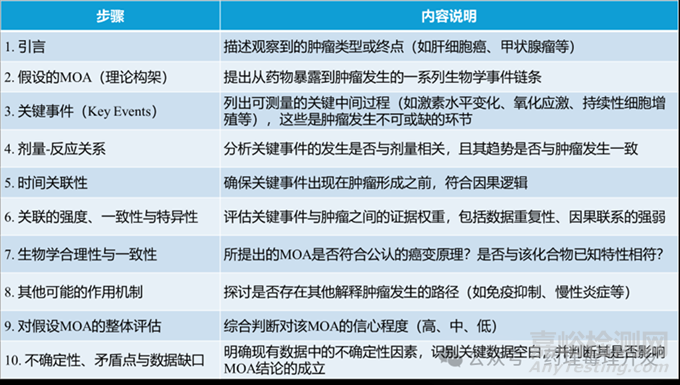
為此,國際化學品安全規(guī)劃署(IPCS)建立了一套系統(tǒng)的MOA分析框架�����,包含以下10個步驟:
這套框架為科學解讀動物致癌性結果提供了系統(tǒng)化、透明化的工具��。
三、判斷動物機制是否適用于人類:人類相關性框架(HRF)
為了進一步評估動物中發(fā)現(xiàn)的致癌機制是否與人類健康相關,國際生命科學學會/風險科學研究所(ILSI/RSI)提出了人類相關性框架(Human Relevance Framework, HRF)���,基于四個核心問題:
若能證明:
·該MOA依賴于僅存在于動物中的生理機制(如大鼠特有的激素調節(jié)通路)�;
·或關鍵事件在人體中無法達到所需水平���;
·或所需暴露濃度遠超臨床劑量���;
則可認為:盡管動物試驗陽性�,但對人體無顯著致癌風險�����。
該“MOA+HRF”聯(lián)合分析方法已被廣泛應用于多種類型的腫瘤和藥物類別(如某些激素類藥物、酶誘導劑����、抗炎藥等)的風險評估����,成為現(xiàn)代藥物安全性評價的重要組成部分。
總結下����,陽性致癌性研究后的決策路徑如下:
四、動物試驗中常見的����、對人類意義存疑的腫瘤類型
盡管長期致癌性試驗是評估藥物潛在致癌風險的重要手段�����,但許多在大鼠或小鼠中觀察到的腫瘤具有物種特異性機制,在人體中并不存在或難以發(fā)生�����。因此��,這些腫瘤的陽性結果不一定提示對人體有致癌風險。
以下是幾類典型的�、被認為與人類相關性較低或無相關性的動物腫瘤示例:
1.F-344大鼠單核細胞白血?��。∕NCL)
僅見于大鼠,尤其常見于F-344品系����。
在國家毒理學計劃(NTP)的研究中�����,未處理對照組的自發(fā)率高達:雄性48.2%�、雌性23.7%����。腫瘤發(fā)展存在明顯閾值效應(即需超過一定暴露水平才出現(xiàn))���。
某些已知的遺傳毒性致癌物并不會增加MNCL發(fā)生率���,而一些非致癌物卻可誘發(fā)其升高。
該腫瘤被認為是大鼠特有的背景病變�����,與人類無關����。
2.α2u-球蛋白相關性腎腫瘤(雄性大鼠特有)
發(fā)生于雄性大鼠近端腎小管細胞,原因是積累了一種雄性大鼠特有蛋白質——α2u-球蛋白���,導致溶酶體功能障礙和細胞持續(xù)增殖����。人類不合成這種蛋白�����,也不存在類似的代謝路徑�。
此類腎腫瘤為雄性大鼠特有機制��,不適用于人類風險評估����。
3.甲狀腺腫瘤(大鼠)
可由干擾“垂體-甲狀腺軸”反饋機制的化合物引發(fā)(如肝酶誘導劑加速T4代謝→TSH代償性升高→甲狀腺增生→腫瘤)。
盡管該通路在人類中也存在���,但存在顯著生理差異:人類血液中有甲狀腺素結合球蛋白(TBG),可穩(wěn)定激素水平���;而嚙齒類缺乏此蛋白。
甲狀腺素(T4)半衰期:大鼠約16小時vs.人類5–9天����。
血清甲狀腺激素水平:嚙齒類約為人類的25倍����,表明其甲狀腺更活躍。
所以,大鼠對甲狀腺刺激更為敏感�,此類腫瘤在人類中的相關性較低�����。
4.膀胱腫瘤(大小鼠)
常因尿液中形成沉淀物引起慢性刺激→上皮增生→惡變。
但人與動物存在關鍵差異:嚙齒類尿液高滲�、高蛋白,易形成結晶或結石��;四足動物(水平體位)結石更容易滯留于膀胱;人類直立體位利于排石�����。
若腫瘤僅在高于沉淀閾值濃度時出現(xiàn)�,且無其他機制證據(jù)��,則認為對人類風險低或無關���。
5.肝腫瘤(大小鼠)
許多非遺傳毒性化合物可在嚙齒類(尤其是小鼠)中誘發(fā)肝腫瘤�����。
可能的作用機制包括:細胞毒性→持續(xù)再生性增殖���;肝酶誘導(如CYP450)��;內分泌紊亂�����;免疫抑制�����;卟啉代謝異常等����。
特別是在小鼠中單獨出現(xiàn)的肝腫瘤,常被認為人類相關性有限����。
需結合MOA分析判斷�����。若機制依賴于小鼠特有反應(如強PXR激動),則可能不適用于人類��。
6.Leydig細胞腫瘤(睪丸間質細胞瘤)
多見于大鼠���,也可發(fā)生于小鼠和比格犬。
常由干擾“下丘腦-垂體-睪丸軸(HPT軸)”的藥物引起�,導致LH(黃體生成素)升高,進而刺激Leydig細胞增生�。
常見誘因包括:雄激素受體激動劑/拮抗劑�����;5α-還原酶抑制劑�����;芳香化酶抑制劑;多巴胺激動劑等���。
雖然HPT軸調控機制在人與大鼠相似�����,但人類對LH升高的反應較弱����。
流行病學數(shù)據(jù)顯示:普通人群中Leydig細胞腺瘤/癌極為罕見�����,且未發(fā)現(xiàn)用藥后發(fā)病率上升�。
總體認為人類男性對此類腫瘤不敏感�,但需個案評估��。
7.子宮腫瘤(大鼠)
實例:溴隱亭(bromocriptine,多巴胺激動劑)
抑制催乳素分泌→打破老齡雌性大鼠持續(xù)動情后期狀態(tài)→引發(fā)異常周期→雌激素/孕激素比例失衡→子宮鱗狀化生→子宮內膜炎�����、積膿→刺激增生→癌變�����。
此過程依賴于老年大鼠特有的內分泌狀態(tài)����。
在犬(52周)和小鼠致癌試驗中均未觀察到類似變化����。
臨床患者子宮內膜活檢也未發(fā)現(xiàn)藥物相關改變。
該腫瘤為老年雌性大鼠特有的藥理放大效應(exaggerated pharmacodynamic effect)���,對女性無相關性。
8.激素紊亂引起的腫瘤
動物體內分泌系統(tǒng)對某些藥物高度敏感�,易引發(fā)激素失衡導致腫瘤(如乳腺��、垂體��、腎上腺等)。
這些效應往往基于嚙齒類特有的內分泌生理特點����,在人類中不易復制��。
所以��,若機制明確為物種特異性激素擾動���,則通常認為不具人體相關性。
9.嚙齒類特有器官的腫瘤:天然無對應結構
以下器官為嚙齒類特有����,在人類中無解剖對應結構,因此其腫瘤通常被視為無臨床意義:
需要注意的是�����,雖然這些器官本身無對應結構,但仍需關注其作用機制是否具有普適性���。例如,前胃腫瘤常由局部刺激引起(如口服灌胃導致高濃度藥物長時間接觸上皮)�,類似于人類食管上皮暴露。但由于人類吞服藥片時接觸時間短�,而動物經(jīng)口灌胃造成持久暴露�。因此��,若非遺傳毒性化合物在遠低于刺激濃度下使用��,則認為對人類無致癌風險。
最后
如何評估動物腫瘤的人類相關性��?
不能僅憑腫瘤發(fā)生與否做判斷��,必須深入分析其MOA���。
對于上述典型腫瘤類型,已有充分科學共識認為其在人類中不具備發(fā)生基礎�。
當遇到新化合物或新型腫瘤時�,應采用“整體證據(jù)權重法”進行個案評估:是否存在物種特異性機制?關鍵事件是否能在人體重現(xiàn)�?是否存在足夠的安全邊際��?
最終目標是區(qū)分:真正具有跨物種致癌潛力的風險信號����;僅為動物模型中的假陽性或生物學噪聲。