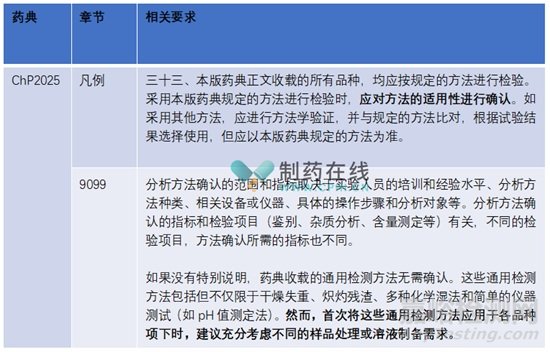
在展開(kāi)本文前���,我們先來(lái)看FDA發(fā)布的兩封483報(bào)告�,報(bào)告中關(guān)于分析方法確認(rèn)的缺陷描述如下:
1.FDA_483_Glenmark_Pharmaceuticals_Ltd_20250214
Commercial drug products and Active Pharmaceutical Ingredients (API) test methods, including in-house and compendial test methods were not validated or verified appropriately. More than products and API are routinely released by testing with analytical test methods that have not been adequately validated or verified. The test methods include method for content, specific optical rotation, identification test by IR, UV and TLC.
內(nèi)控或藥典方法未進(jìn)行驗(yàn)證或確認(rèn)�,包括比旋、紅外���、紫外����、TLC等�����。
2.FDA_483_Dr_Reddy's_Laboratories_Limited_CTO__Unit_VI_20240607
Analytical methods were not validated or verified under the actual conditions of use. These methods are used for testing official Active Pharmaceutical Ingredients (API) before releasing the APIs for the manufacturing of drug products.
The following test methods, including in-house and compendial test methods, were not validated or verified appropriately for the commercial APIs. These APIs have active US Drug Master Files (DMF) and batches were distributed to customers and are currently in the market.
紅外���、鑒別���、水分�、旋光度等分析方法未進(jìn)行驗(yàn)證或確認(rèn)。
總結(jié):分析方法應(yīng)經(jīng)過(guò)驗(yàn)證或確認(rèn)�,即使是通用性的檢測(cè)方法也應(yīng)該確認(rèn)在實(shí)驗(yàn)室的適用性。
● 什么是分析方法確認(rèn)
分析方法確認(rèn)(analytical method verification) 是指首次使用法定分析方法時(shí)�����,由現(xiàn)有的分析人員或?qū)嶒?yàn)室對(duì)分析方法中關(guān)鍵的驗(yàn)證指標(biāo)進(jìn)行有選擇性的考察,以證明方法對(duì)所分析樣品的適用性����,同時(shí)證明分析人員有能力使用該法定分析方法。
分析方法驗(yàn)證(Analytical Method Validation):指實(shí)驗(yàn)室通過(guò)試驗(yàn)設(shè)計(jì)和檢測(cè)����,證明建立的方法適合用于相應(yīng)擬定的檢測(cè)用途。在建立藥品質(zhì)量標(biāo)準(zhǔn)�����、變更藥品生產(chǎn)工藝或制劑組分��、修訂原分析方法時(shí)���,需對(duì)分析方法進(jìn)行驗(yàn)證���。
本圖為USP 1058中QC實(shí)驗(yàn)室數(shù)據(jù)的金字塔,分析方法驗(yàn)證或確認(rèn)是方法正式實(shí)施前的重要一部分����。
● 藥典及法規(guī)指南中相關(guān)要求
總結(jié):實(shí)施藥典方法前���,使用者應(yīng)評(píng)估藥典方法在實(shí)際條件的適用性或適用的程度,如果沒(méi)有特別說(shuō)明�,藥典收載的通用檢測(cè)方法無(wú)需確認(rèn)。但首次將這些通用檢測(cè)方法應(yīng)用于各品種項(xiàng)下時(shí)��,建議充分考慮不同的樣品處理或溶液制備需求�����,應(yīng)形成評(píng)估文件�。
● 藥典分析方法確認(rèn)的評(píng)估如何進(jìn)行(5.26 IMPLEMENTATION OFPHARMACOPOEIAL PROCEDURES)
1、 分析方法性能的關(guān)鍵因素識(shí)別
主要從以下方面的因素進(jìn)行評(píng)估:
● 待測(cè)物品的組成(是否純物質(zhì)���、樣品組分�����、溶解度�����、引濕性等)
● 樣品制備的復(fù)雜性(制備過(guò)程是否復(fù)雜,實(shí)驗(yàn)室是否有類似操作)
● 方法所需的試劑(實(shí)驗(yàn)室是否可得�,是否是常用化學(xué)試劑�����,試劑的適用性是否經(jīng)過(guò)確認(rèn)等)
● 方法所需的實(shí)驗(yàn)室設(shè)備(儀器設(shè)備是否是實(shí)驗(yàn)室常用設(shè)備)
● 實(shí)驗(yàn)室環(huán)境(溫濕度控制�����、光照控制等)
● 各論和相關(guān)通則中規(guī)定的條款����,例如適用性要求或其他描述的性能測(cè)試�����。
2����、分析方法性能指標(biāo)評(píng)估
關(guān)鍵因素評(píng)估后,有兩種可能的結(jié)果:
1. 如果未識(shí)別出任何關(guān)鍵因素��,則程序可在實(shí)施實(shí)驗(yàn)室中使用�����,無(wú)需進(jìn)行任何特定的驗(yàn)證實(shí)驗(yàn)以證明其在實(shí)際使用條件下的適用性����;
2. 如果識(shí)別出關(guān)鍵因素�,則該程序可在實(shí)施實(shí)驗(yàn)室中使用�����,前提是需開(kāi)展一組驗(yàn)證實(shí)驗(yàn)�,評(píng)估所識(shí)別的關(guān)鍵因素對(duì)選定APPCs(分析方法性能指標(biāo))的影響,以證明分析程序在實(shí)際使用條件下的適用性����。
需進(jìn)行確認(rèn)
如果實(shí)驗(yàn)室實(shí)際條件下存在影響因素,需進(jìn)行確認(rèn)
無(wú)需進(jìn)行確認(rèn)
總結(jié):藥典方法在實(shí)驗(yàn)室使用前應(yīng)進(jìn)行評(píng)估和識(shí)別是否存在影響分析方法性能的關(guān)鍵因素�,如果未識(shí)別出任何關(guān)鍵因素,則程序可在實(shí)施實(shí)驗(yàn)室中使用���,無(wú)需進(jìn)行任何特定的驗(yàn)證實(shí)驗(yàn)以證明其在實(shí)際使用條件下的適用性���;如果識(shí)別出關(guān)鍵因素,則該程序可在實(shí)施實(shí)驗(yàn)室中使用���,前提是需開(kāi)展一組驗(yàn)證實(shí)驗(yàn)�,評(píng)估所識(shí)別的關(guān)鍵因素對(duì)選定APPCs(分析方法性能指標(biāo))的影響���,以證明分析程序在實(shí)際使用條件下的適用性���,具體確認(rèn)的項(xiàng)目應(yīng)結(jié)合具體的檢測(cè)項(xiàng)目需求。